2018年生物医药行业市场现状与发展趋势分析,FDA获批肿瘤药数量增加【组图】
现阶段,受各渠道化学致癌因素的增加,不良生活习惯导致免疫力低下及环境污染加剧等内外因共同作用下,全球范围内癌症患病率和发病率都有不同程度的提升。各国相关药品研发生产企业根据市场需求的变动也迅速做出反应,增加对肿瘤药的研发,而美国食品药品监督管理总局FDA也根据实际情况增加了对抗肿瘤药审批的关注。
2018年,获批抗肿瘤新药创历年新高
从获得审批的具体新药请情况看, 2018年FDA新药评审中心(CDER)共批准了59个新药,其中新分子实体42个,生物制品17个,该数据打破了1996年批准53个新药的纪录。
从获批新药的治疗领域看,抗肿瘤新药是目前重要的关注领域。除2016年抗肿瘤新药获批数量仅为5种外,从2014年起FDA通过肿瘤新药数量呈稳步上升趋势;2018年FDA通过的16种肿瘤新药中,治疗实体肿瘤新药的比例超过50%。

2014-2018年FDA通过的肿瘤药物分类占比图显示,2016年后FDA对肿瘤药物的审批越来越关注非实体瘤领域。2018年,FDA批准的肿瘤新药中,治疗实体瘤新药有9种,占比56.25%,非实体瘤药物7种,占比43.75%,基本持平。

抗肿瘤新药为各评审方法的重要关注领域
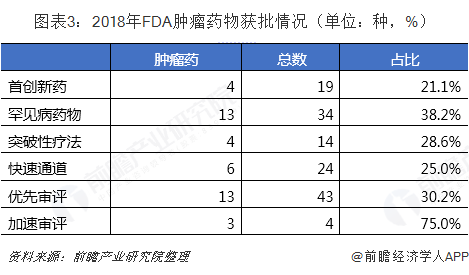
2018年59种新药批准中,43种(73%)被指定为四种审评方式种的一个或多个类别,其中优先审查24种(41%),14种(24%)为突破性疗法,43种(73%)为优先审查,4种(7%)加速批准。
从获批抗肿瘤药不同审批方法看,首创型肿瘤药4中,罕见病肿瘤药物13种。都是该审批方法中占有较高比例的获批新药。除此之外,有13种抗肿瘤药获得优先审批,占比30.2%。在全年4个获得加速审批通过的新药中,其中3个都为肿瘤药物。由此可见肿瘤药的审批获得FDA的重点关注。
白血病为获批抗肿瘤新药的主要适应症
肿瘤,由于其种类众多、致病原因不一、复发率高,成为长期困扰人们的疾病之一。近年来,FDA对肿瘤药物的批准呈稳步上升趋势。在2018年FDA发布的《报告》中,FDA共批准了肿瘤新药和肿瘤类似生物药19个。其中肿瘤新药16种,以美国企业申请为主,白血病为获批药品的重要关注领域,其大多处在临床III期。而肿瘤生物类似药品3种,多为美国FDA生物制品许可申请为主。

2018年,获批抗肿瘤新药的详细解读
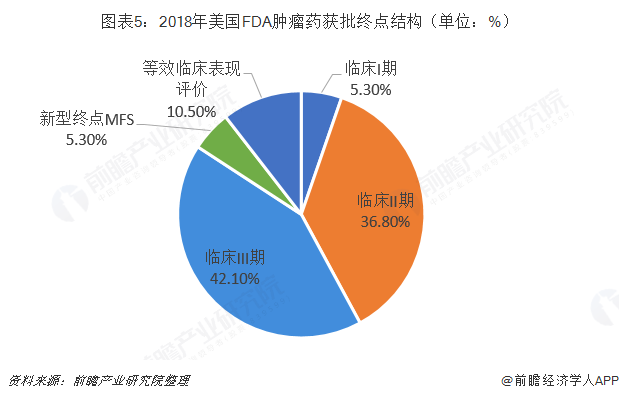
临床III期为获批新药主要终点
从获批肿瘤药不同的终点情况看,主要表现为临床II期、临床III期,其中基于临床Ⅱ期获批的有7种,占比36.8%;基于临床Ⅲ期获批的有8种,占比42.1%;基于等效临床表现评价获批的生物类似药有2种,占比10.6%。除此之外,基于临床Ⅰ期和基于新型终点MFS获批的新药均为1种,占比5.3%。
美国药企为主要申报单位
从获批抗肿瘤新药的申请单位看,美国药企为主要的申请单位,以ARRAY、VERASTEM、辉瑞和强生等美国著名的药品生产企业为代表。2018年获得FDA批准的16个肿瘤新药+3个肿瘤生物类似药品中,美国本土品牌申请数量为14个,遥遥领先。法国、日本和瑞士企业申请成功的抗肿瘤药品数量分别为2个和1个。

NDA新药为主要产品类型
美国FDA审批通过的抗肿瘤药主要分为新药申请(NDA)和生物制品许可药(BLA)两种,其中NDA为抗肿瘤药的主要产品类型。2018年获批的19种抗肿瘤相关药品中,NDA抗肿瘤药为13种,占获批药品数量的68.42%;BLA药品6种,占比31.58%。

以上数据来源参考前瞻产业研究院发布的《中国生物医药行业市场前瞻与投资战略规划分析报告》。
更多深度行业分析尽在【前瞻经济学人APP】,还可以与500+经济学家/资深行业研究员交流互动。
前瞻产业研究院 - 深度报告 REPORTS
本报告前瞻性、适时性地对生物医药行业的发展背景、供需情况、市场规模、竞争格局等行业现状进行分析,并结合多年来生物医药行业发展轨迹及实践经验,对生物医药行业未来...
如在招股说明书、公司年度报告等任何公开信息披露中引用本篇文章数据,请联系前瞻产业研究院,联系电话:400-068-7188。
品牌、内容合作请点这里:寻求合作 ››

前瞻经济学人
专注于中国各行业市场分析、未来发展趋势等。扫一扫立即关注。



























