2018年生物医药行业市场现状与发展分析 新药加速获批【组图】
生物医药的发展关系各国民生,因此全球范围内重视药物审批的权威性、科学性。目前,全球形成了以美国FDA、欧盟EMA、日本PMDA、中国CFDA,四大全球主要审评机构为代表的新药审批机构为代表的全球新药审批的发展情况,从近年来新药获批情况看,各权威机构的新药获批的进度都有不同程度的增加。
FDA新药获批数量能加,罕见药增加明显
据美国FDA统计数据显示,2010-2018年,美国FDA新药审批结构对NDA/BLA受理批准总新药数量不断增加,截止至2018年12月18日,美国NDA/BLA受理批准总数量达148件,较2017年增加3项。

注:数据截止至2018年12月17日
从获得审批的具体新药请情况看,2000年以来,新药获批总体呈上升趋势,2014年后生物制品新药获批数量大幅增加。2018年FDA新药评审中心(CDER)共批准了59个新药,其中新分子实体42个,生物制品17个,该数据打破了1996年批准53个新药的纪录。
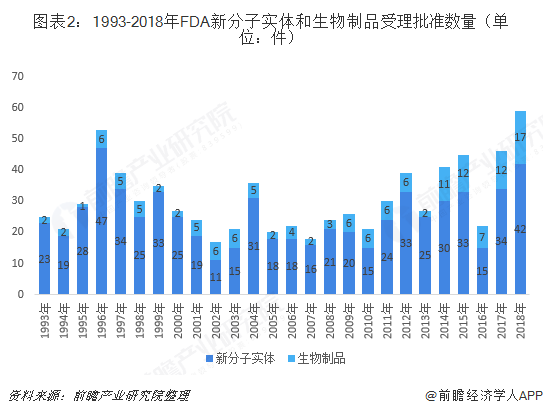
从历年FDA批准的新药品种看,2018年获批新药的数目却首次未由抗癌疗法所主导。重视对罕见病药物的审批,数据显示,2018年共有31款治疗罕见疾病的新药获批,占比55%,创下了历史新高。美国相关机构报告指出,2018年创新分子实体中,大部分是治疗罕见疾病的孤儿药。

新分子实体药商业前景广阔,16个药品峰值超10亿
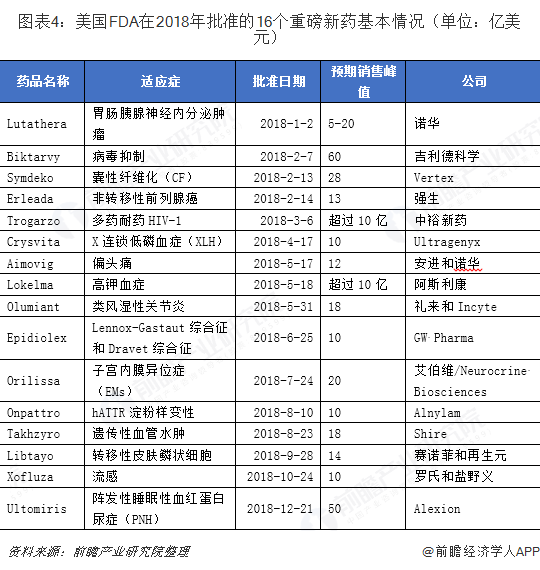
在2018年,美国食品和药物管理局(FDA)共批准了59个新分子实体(NME),打破了过去20多年的最高记录(1996年53个)。与以往NME主要集中在肿瘤学领域不同,2018年是有史以来第一次大多数NME用于治疗罕见病,59个NME中就有33个是孤儿药。权威机构对这59个NME的商业前景进行了分析,其中16个NME的预期销售峰值或将突破10亿美元,具体产品和相关分析如下。
EMA新药获批数量大幅增加,创新药批准获关注
截止到2018年12月18日,欧盟NDA/BLA受理批准总数量达79件,刷新了历年的批准记录。其中包含化学小分子创新药物(NME)18件,生物大分子创新新药物16件,细胞疗法类3件,疫苗类1件。创新药物批准数量总和达到34件,较往年相对平稳。

注:数据截止至2018年12月17日
在一系列鼓励创新、加速审评政策之下,2018年,中国新药也有了很大突破。中国批准48个全新药品上市,其中38个来自进口、10个来自国产,涉及的适应症有多发性骨髓瘤、非小细胞肺癌、宫颈癌、卵巢癌、乳腺癌、黑色素瘤、肝癌、直肠癌、前列腺癌、白血病和淋巴瘤等。从各国新药审批权威机构的审批情况看,肿瘤新药和罕见病新药的审批关注度较高。
以上数据来源参考前瞻产业研究院发布的《中国生物医药行业市场前瞻与投资战略规划分析报告》。
更多深度行业分析尽在【前瞻经济学人APP】,还可以与500+经济学家/资深行业研究员交流互动。
前瞻产业研究院 - 深度报告 REPORTS
本报告前瞻性、适时性地对生物医药行业的发展背景、供需情况、市场规模、竞争格局等行业现状进行分析,并结合多年来生物医药行业发展轨迹及实践经验,对生物医药行业未来...
如在招股说明书、公司年度报告等任何公开信息披露中引用本篇文章数据,请联系前瞻产业研究院,联系电话:400-068-7188。
品牌、内容合作请点这里:寻求合作 ››

前瞻经济学人
专注于中国各行业市场分析、未来发展趋势等。扫一扫立即关注。




























